Normaal gesproken volgt een stamceltransplantatie wanneer bij de geboorte het immuunsysteem niet werkt. Een internationaal onderzoeksteam onder leiding van het Leids Universitair Medisch Centrum (LUMC) krijgt 6 miljoen euro uit het Europese Horizon2020-programma voor hun onderzoek naar een veelbelovend alternatief: het corrigeren van het foutje in het DNA.
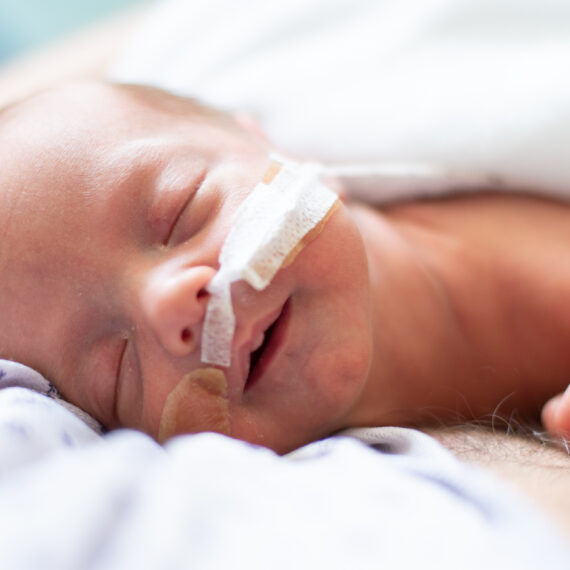
Bij kinderen met de zeldzame aangeboren afwijking severe combined immunodeficiency syndrome (SCID) werkt het afweersysteem niet. Dat komt door een fout in het DNA. De kinderen zijn ontzettend vatbaar voor levensbedreigende infecties en overlijden zonder behandeling voor hun eerste levensjaar. De standaardbehandeling is een stamceltransplantatie. “Maar dit is niet voor alle kinderen een ideale oplossing”, aldus hoogleraar Kindergeneeskunde en Stamceltransplantatie Arjan Lankester.
Niet optimaal
Vooral voor baby’s voor wie geen passende donor gevonden wordt, is de uitkomst van stamceltransplantatie vaak niet optimaal. “In die situatie is het alsof je de kapotte motor van een Peugeot vervangt met die van een Volvo die nog achterin de garage lag. Het werkt vaak wel, maar helemaal lekker loopt de auto niet meer. Liever zou je het kapotte onderdeel van de Peugeot-motor vervangen.” En dat laatste is precies de insteek van de studie waarvoor hij en zijn collega Frank Staal, hoogleraar Moleculaire stamcelbiologie van de afdeling Immunohematologie en Bloedtransfusie (IHB), de Europese subsidie van 6 miljoen euro kregen. Ook de ziekenhuisapotheek en de afdeling Medische Besliskunde doen mee aan dit onderzoek.
DNA-foutje corrigeren
In samenwerking met een aantal prominente kindertransplantatiecentra in Europa gaan de onderzoekers het probleem bij de kern aanpakken door het DNA-foutje te corrigeren. “Dat doen we met gentherapie: we gebruiken een verzwakt virus om een gezonde kopie van het defecte gen toe te voegen aan het DNA aan de eigen stamcellen van kinderen met SCID”, legt Staal uit. Als deze cellen worden teruggegeven aan patiënten, zou daaruit een gezond afweersysteem moeten groeien. “Dat dit in ons laboratorium mogelijk is, is voor een belangrijk deel toe te schrijven aan de inzet van onze senior-onderzoeker Karin-Pike Overzet. Zij is essentieel voor ons gentherapie-onderzoek”, aldus Staal.
Gentherapie heeft meerdere voordelen boven een stamceltransplantatie, denken de onderzoekers. “Doordat we lichaamseigen stamcellen gebruiken, hebben we niet te maken met complicaties door een niet-passende donor en graft-versus-host-ziekte, waarbij de nieuwe afweercellen het lichaam van de ontvanger aanvallen”, legt Lankester uit.
Reizende therapie
Het unieke van hun studie zit hem volgens de LUMC-onderzoekers in de opzet. “We werken samen met alle Europese experts op het gebied van gentherapie en stamceltransplantatie”, zegt Lankester. Ruim een derde van de 6 miljoen euro gaat naar het LUMC, omdat Lankester en Staal vanuit daar de studie coördineren. “Stamcellen van buitenlandse patiënten worden afgenomen in het eigen ziekenhuis, in ons laboratorium bewerkt en vervolgens teruggestuurd naar de partners in Europa. We laten dus niet de patiënt reizen, maar de therapie.”
Bron: lumc.nl